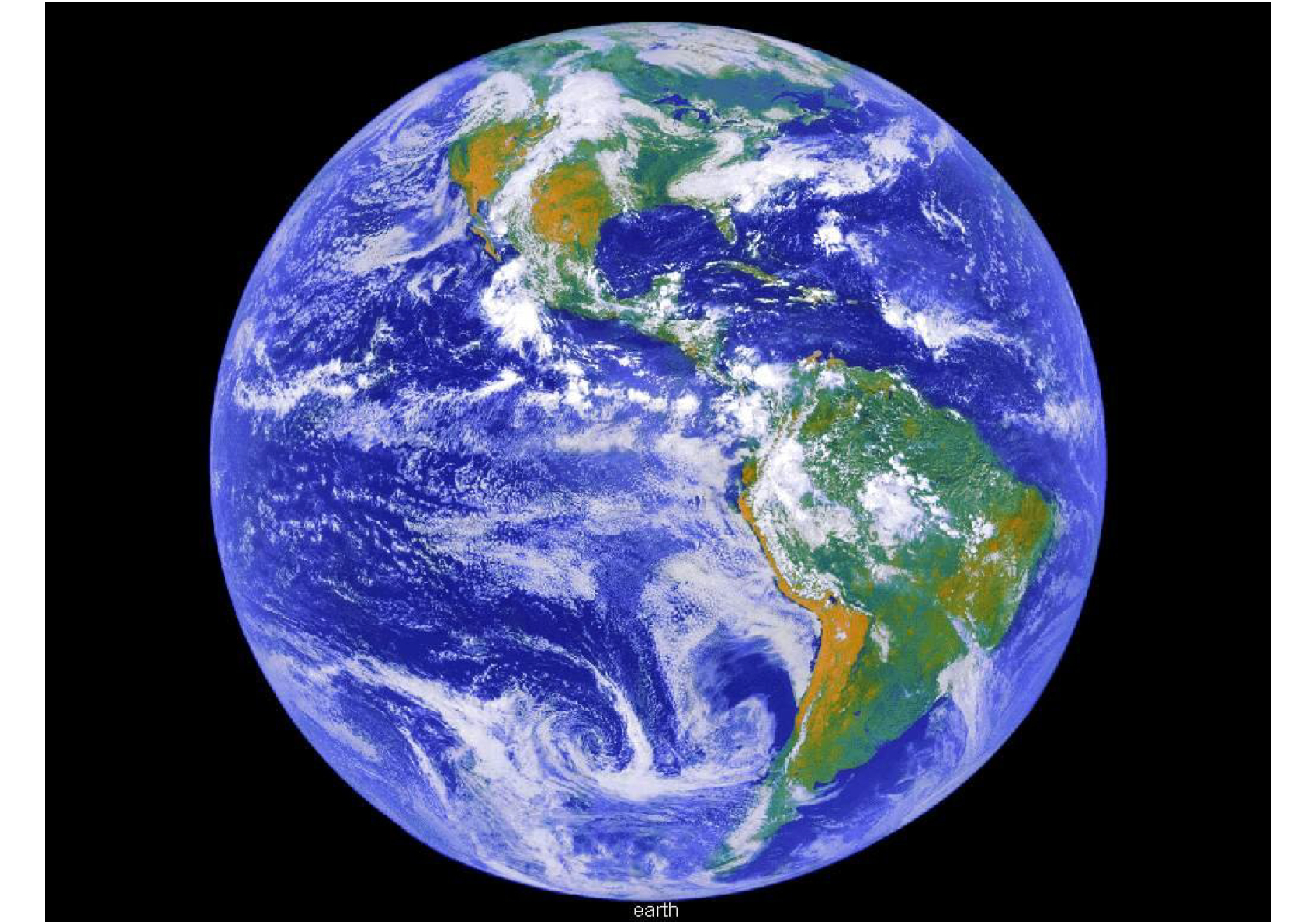
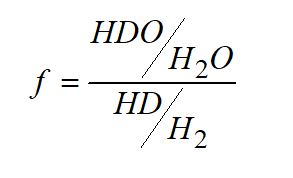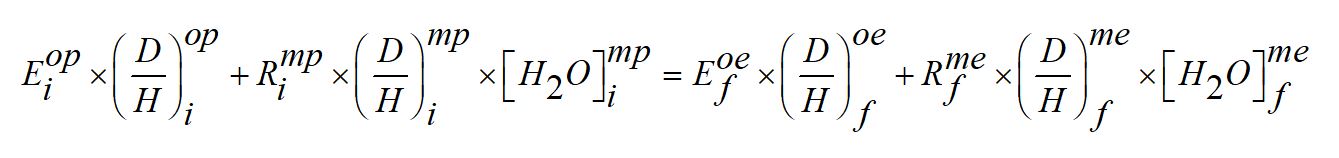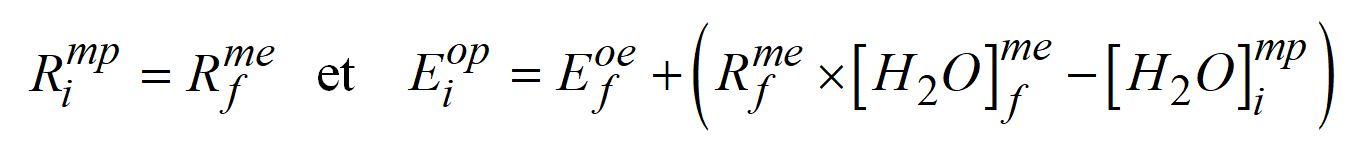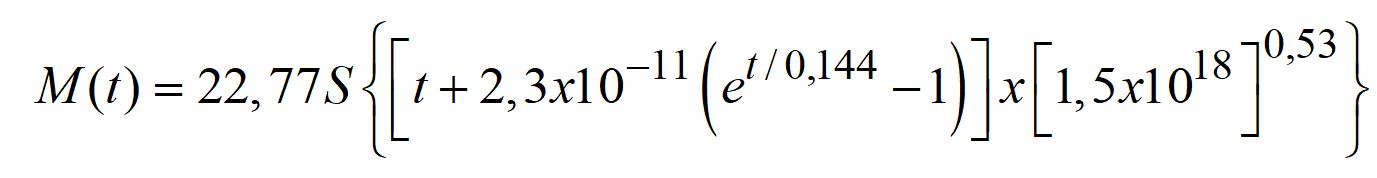1. La Planète bleue du système solaire
Quelle est l’origine des théories qui évoquent l’existence sur Terre d’une eau extraterrestre pour expliquer l’existence des océans de notre planète ? L’eau sur Terre est en effet en quantité énorme par rapport aux autres planètes telluriques du système solaire. Ces planètes telluriques sont principalement composées de matériaux hautement réfractaires (dont le point de fusion est élevé, proche de 1 000°C), elles se sont formées dans la région intérieure du système solaire, là où les températures ont été suffisamment élevées pour empêcher la présence de quantités importantes de substances volatiles telles que de l’eau pendant les processus de condensation et l’accrétion de planétésimaux. Aujourd’hui toutefois, Mars et Vénus ne contiennent que de petites quantités d’eau dans leurs enveloppes extérieures par rapport aux quantités énormes présentes sur Terre, soit 1,38×1021 kg (figure 1 et voir chapitre 3).
Au début de son histoire, Mars a probablement connu l’existence de couches minces et clairsemées d’eau, la plupart d’entre elles ont probablement disparu aujourd’hui, consommées par l’oxydation des basaltes (processus qui a contribué, par formation d’oxyde de fer, type hématite rouge, à lui donner son célèbre surnom de « planète rouge »), le dihydrogène moléculaire résiduel s’étant échappé de la surface de Mars en raison de sa trop faible gravité, contrairement aux planètes géantes comme Jupiter ou Saturne. L’orbite de Vénus est relativement proche du Soleil et on peut s’interroger sur la quantité d’eau hébergée par cette planète au début de son histoire car celle-ci aurait faciliter le stockage du CO2 atmosphérique sous forme de minéraux carbonatés comme cela s’est produit sur Terre quand les océans ont commencé à se former, moins de 100 millions d’années après le processus d’accrétion des plané-tésimaux rocheux. Dès lors que ce CO2 n’a pas été piégé, il s’est accumulé dans l’atmosphère et est responsable de l’énorme effet de serre actuel, entraînant des températures de surface atteignant environ 470°C en moyenne.
Figure 1. 71 % de la surface de la Terre est couverte par des océans
La masse actuelle de l’eau à la surface de Vénus est de seulement 6×1015 kg. Cela signifie-t-il néanmoins que l’on peut faire l’hypothèse que la Terre et Vénus présentaient initialement de grandes différences de teneurs en eau ? C’est peu probable, car les collisions entre planétésimaux ont dû donner naissance, à des distances du Soleil comprises entre 0,5 et 1,5 UA (unités astronomiques), à un mélange homogène, conduisant à des contenus en éléments volatiles (dont l’eau) similaires dans la Terre comme dans Vénus.
Il convient par conséquent de considérer une autre hypothèse, basée sur le fait que les deux planètes ont bien initialement reçu, toute proportion de masse gardée, des quantités identiques d’eau, stockée à l’intérieur ou absorbée à la surface des corps parents qui leur ont donné naissance, astéroïdes primitifs formés au cours de la genèse du système solaire. Normalisée à la masse de la Terre, la quantité initiale d’eau sur Vénus aurait ainsi été proche de 1,2×1021 kg. Par ailleurs, le rapport isotopique D/H élevé (2,5×10-2) mesuré dans l’atmosphère de Vénus, comparé à celui de la Terre qui est de 149 ± 3×10-6, suggère que la planète Vénus peut avoir abrité à sa surface plus d’une centaine de fois plus d’eau qu’elle n’en présente dans son atmosphère actuelle. L’hypothèse est que cette eau primordiale aurait été perdue par photodissociation suivie d’une évasion hydrodynamique de l’hydrogène vers l’espace interplanétaire. Si cette eau de surface a bien disparu par ces deux processus, la masse initiale d’eau de 1,2×1021 kg aurait laissé 1,07×1021 kg d’oxygène moléculaire dans l’atmosphère vénusienne, non susceptible de connaître une évasion hydrodynamique. A la température de surface de Vénus, l’oxydation des roches basaltiques par cet oxygène peut alors être formulée comme suit :
2 FeSiO3 + 1/2O2 = Fe2O3 + 2 SiO2
Ferrosilite Hématite Quartz
La ferrosilite, l’hématite et le quartz étant les composants des minéraux des basaltes comme les pyroxènes ou les spinelles.
La modélisation thermodynamique de la réaction minéralogique ci-dessus, en utilisant une procédure de minimisation de l’énergie libre, peut prédire la stabilité de l’hématite dans les conditions de P et T de la surface de Vénus. La stœchiométrie de cette réaction implique l’oxydation de 5,3×1022 à 6,9×1022 kg de basalte en supposant une concentration moyenne de 7 à 9 % de FeO dans les basaltes vénusiens, oxydation sur une épaisseur de la croûte atteignant 50±10 km. L’oxydation des roches de surface de Vénus avec formation de minéraux ferriques a été proposée dès 1982, sur la base de l’analyse des images multispectrales obtenues par le vaisseau spatial soviétique Venera 13.
L’hypothèse de l’existence d’une masse d’eau primordiale importante sur Vénus conduit également à étudier par analogie les réactions d’hydratation possibles de roches basaltiques se produisant sur Terre lors des interactions hydrothermales entre l’eau de mer et les roches basaltiques.
Des calculs thermodynamiques ont donc été effectués dans des gammes de P et T qui correspondent à la fois aux conditions de surface (T = 660 à 760 K ; P = 48 à 100 bars) et de subsurface (avec un gradient thermique de 10 à 30 K.km-1 jusqu’à 40 km de profondeur) de Vénus. Par exemple, la serpentine (Mg3(OH)4(Si3O5), le talc ((Mg3Si4O10(OH)2) et la chlorite ((Fe, Mg, Al)6(Si, Al)4O10(OH)8), qui contiennent de 10 à 15 % en poids de H2O, sont stables dans une atmosphère de 100 bars de CO2 lorsque l’eau est abondante. Des amphiboles magnésiennes, comme la trémolite (Ca2Mg5Si8O22(OH)2) et le mica phlogopite (KMg3(Si3Al)O10(F, OH)2), qui contiennent environ 4 % en poids de H2O, sont également stables, même lorsque l’eau ne représente que quelques pour cent de l’enveloppe fluide.
L’hydratation sur une épaisseur de 10 à 30 km de la croûte vénusienne est nécessaire pour piéger 1,2×1021 kg d’eau dans la stoechiométrie de ces minéraux hydratés. Le phlogopite n’est qu’une phase mineure dans les roches basaltiques pauvres en K. La trémolite pourrait être la dernière phase minérale hydratée à cristalliser à la surface de Vénus, laissant une masse d’eau résiduelle dans l’atmosphère se situant entre 1018 et 2×1018 kg. Environ un million d’années est nécessaire pour la serpentinisation (hydratation/oxydation par l’eau de mer) d’une couche basaltique de 1 km d’épaisseur à 300°C. Aux températures de surface vénusienne, on prévoit que ce taux de serpentinisation doit être supérieur d’au moins un ordre de grandeur, ce qui donne un temps caractéristique d’un million d’années pour l’hydratation de dix kilomètres de croûte basaltique vénusienne. De futures explorations de Vénus aideront à valider ou non l’hypothèse sur les quantités initiales d’eau qui prévalaient lors de la formation de cette planète.
Il est néanmoins nécessaire d’envisager l’hypothèse selon laquelle la Terre et Vénus auraient pu avoir des masses d’eau primordiale très différentes au début de leur histoire. La grande quantité d’eau sur Terre pourrait par exemple résulter d’événements catastrophiques comme des successions de collisions avec les comètes qui parcourent le système solaire.
2. Les comètes
Les comètes sont de petits corps du système solaire composés de glace et de poussières, de faible densité (≈ 600 kg.m-3), avec des masses allant de 1013 à 1014 kg (figure 2). Ils se déplacent rapidement (≈ 100 000 km par heure) sur des orbites elliptiques autour du Soleil, qui recoupent celles des huit planètes du système solaire. Les périodes orbitales de la plupart des comètes vont de quelques décennies à des milliers d’années. Deux grandes classes de comètes ont été documentées à ce jour. D’abord les comètes à courtes périodes, celles appartenant à la « famille de Jupiter », qui sont le moins abondantes et celles qui trouvent très probablement leur origine dans la ceinture d’Edgeworth-Kuiper, au-delà de Neptune. Les comètes à longues périodes sont, elles, formées dans le nuage d’Oort, à mi-chemin environ de l’étoile la plus proche, la naine rouge Proxima du Centaure, située dans la constellation du Centaure. Ces comètes sont constituées d’un noyau rocheux entouré d’une enveloppe composée principalement de poussière, d’eau, de dioxyde et de monoxyde de carbone, de méthane et d’ammoniac, l’ensemble de ces volatiles étant, vu les conditions de température, à l’état de glace solide. L’eau constitue environ 80 % en poids de la masse totale d’une comète.
L’hydrogène est l’atome le plus abondant dans l’Univers, formé au cours du Big Bang, mais son isotope lourd, le deutérium, fabriqué lui quelques minutes après le Big Bang, est très rare, et s’est trouvé concentré dans des molécules organiques et dans l’eau lors de réactions moléculaires de basses températures où des espèces chargées réagissent avec d’autres espèces neutres qui se sont produites dans le nuage présolaire à des températures allant de 10 K à 100 K.
Figure 2. Les comètes, riches en eau, sont de potentielles contributrices
à la genèse des océans terrestres primordiaux
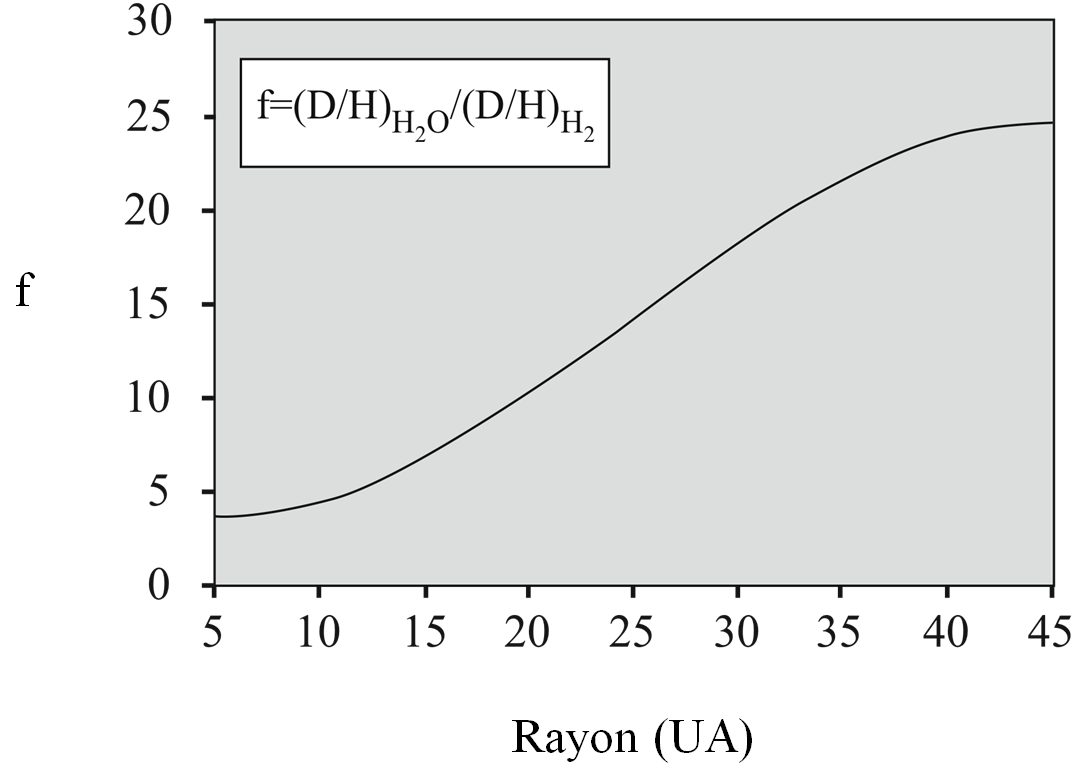
Ces procédés chimiques sont enregistrés et « fossilisés » dans les météorites et les comètes. Dans la nébuleuse solaire nouvellement développée, le degré d’enrichissement du deutérium dans l’eau augmente avec la distance entre le jeune Soleil (figure 3). La réaction d’échange isotopique peut être formulée comme suit :
H2O + HD ⇆ HDO + H2
Figure 3. Variation du facteur f d’enrichissement en deutérium de l’eau condensée,
en fonction de la distance au Soleil. Illustration d’après Horner et al. [HOR 07]
Cette réaction favorise l’enrichissement isotopique en D de la molécule HDO, enrichissement qui est limité par la cinétique réactionnelle, elle-même contrainte par les très faibles températures du milieu de réaction. Le facteur d’enrichissement en D, f, est défini comme le rapport du rapport isotopique D/H entre l’eau et l’hydrogène moléculaire, selon l’équation suivante :
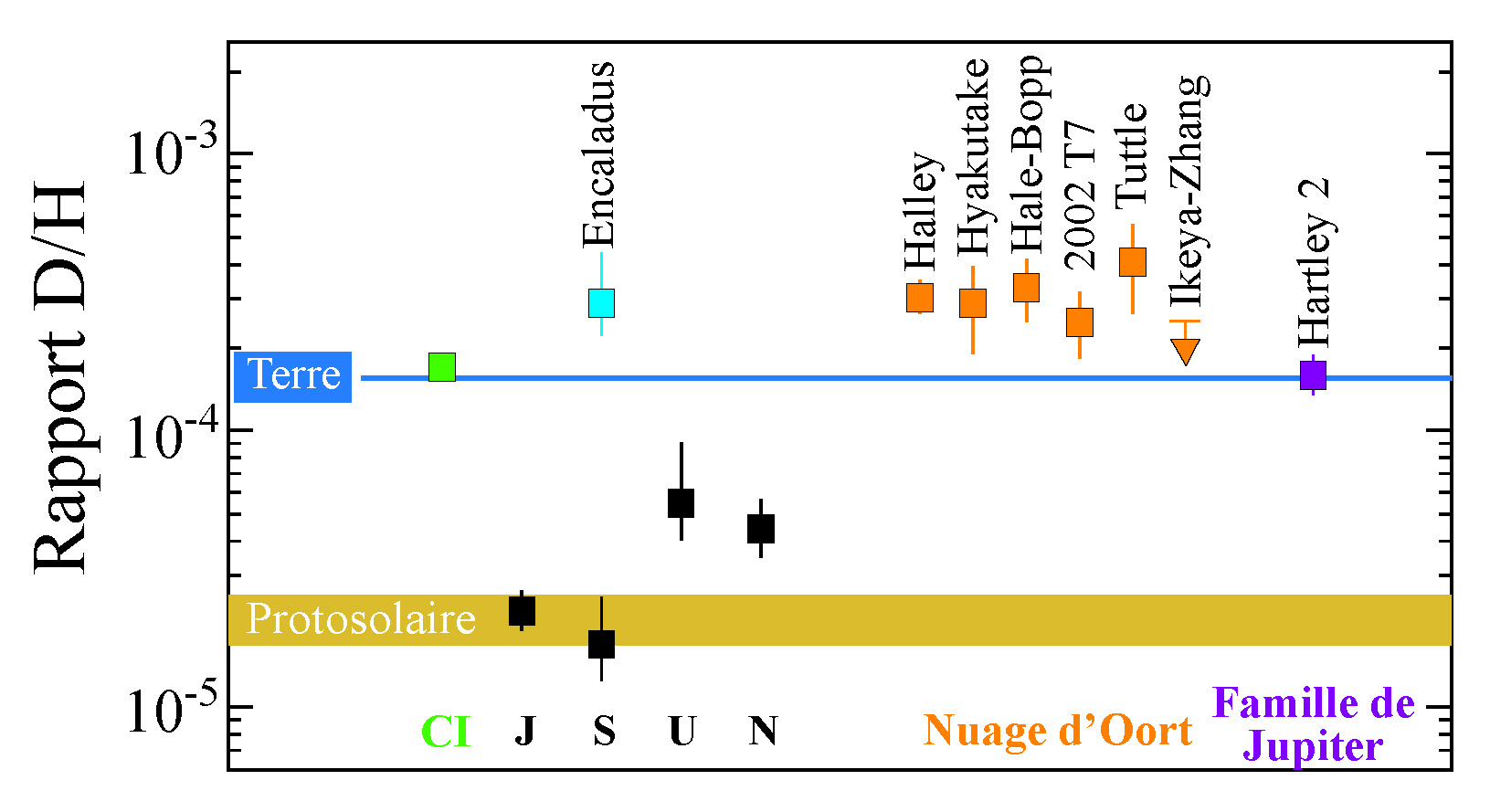
Les comètes ont ensuite conservé pendant des milliards d’années les rapports isotopiques D/H qu’elles ont acquis dans leur région de formation, avec une abondance du deutérium dans la comète corrélée positivement avec la distance héliocentrique. Par conséquent, les comètes à longue période, qui ont été générées dans le nuage d’Oort, loin du Soleil, ont des rapports D/H très élevés, environ deux fois plus que ceux des océans terrestres actuels (D/H = 155,7×10-6) ou de la Terre totale (D/H estimé = 149±3×10-6). Par exemple, les comètes Halley, Hale-Bopp et Hyakutake ont respectivement des rapports isotopiques du deutérium de 316 ± 34×10-6, 320 ± 120×10-6 et 290 ± 100×10-6 (figure 4).
Figure 4. Rapports isotopiques du deutérium des planètes géantes gazeuses,
de la nébuleuse protosolaire, de la Terre et des comètes
(illustration d’après Hartogh et al. [HAR 11])
COMMENTAIRES DE LA FIGURE 4.– Carrés gris clairs : rapports D/H pour l’eau dans les comètes originaires du nuage de Oort, qui sont : 1P/Halley, C/1996 B2 (Hyakutake), C/1995 O1 (Hale-Bopp), C/2002 T7 (LINEAR) et 8P/Tuttle. Le rapport D/H dans les comètes de la « famille de Jupiter », 103P/Hartley 2 est identique à celui des océans de la Terre. Carrés gris foncés : rapport D/H dans l’atmosphère des planètes géantes Jupiter (J), Saturne (S), Uranus (U) et Neptune (N). Carrés dans le coin supérieur de gauche : D/H de l’eau dans le panache de la lune Encelade de Saturne et dans les chondrites carbonées de type CI, respectivement.
En raison de leur enrichissement en deutérium, ces comètes ne peuvent pas avoir été les principaux contributeurs de l’eau sur la Terre. En effet, le rapport isotopique D/H de l’énorme masse océanique est une signature isotopique robuste de son origine. En outre, il n’y a aucun réservoir solide ou fluide sur Terre qui a pu être en mesure de modifier la composition isotopique de l’océan mondial dans le temps, ni par transfert de masse, ni par échange isotopique. De même, toute l’eau parvenue sur Terre a dû conserver la signature isotopique des impactants contributeurs, puisque le fractionnement isotopique du deutérium entre la glace et la vapeur d’eau lors des processus de sublimation est négligeable. Le processus de dissociation photochimique de l’eau est un phénomène naturel qui se produit dans la haute atmosphère. Il provoque donc un flux net de fuite d’hydrogène vers l’espace interplanétaire d’environ 2×108 atomes H.cm-2.s-1, ce qui correspond à un flux d’eau de 8×108 kg.a-1. Ce flux est de trois ordres de grandeur plus faible que les flux d’eau qui affectent le système océan-manteau terrestre et ne peut donc pas affecter de manière significative la masse de l’hydrosphère. En supposant que l’hydrogène est perdu uniquement sous forme de H, sans aucun D, le rapport isotopique D/H de l’océan mondial n’aurait pas augmenté de plus de 10 % de sa valeur initiale pendant les 4,5 milliards d’années d’existence de la Terre.
Il a été récemment proposé que les comètes aux plus courtes périodes orbitales, formées dans la région de Jupiter, dites pour cela joviennes, sont les seules à présenter des rapports D/H compatibles avec la composition isotopique globale de la Terre. Ces comètes ont été générées à des températures proches de 100 K permettant davantage d’échange isotopique avec l’hydrogène protosolaire. La comète Hartley 2, par exemple, a un rapport D/H similaire à celui de la Terre. Ces comètes joviennes pourraient donc bien être les sources d’eau extraterrestres « livrées » sur Terre. Sur la base de l’observation du fait que les rapports isotopiques D/H de l’eau des météorites carbonées et des comètes sont très proches, il semble maintenant raisonnable d’admettre que ces corps puissent être considérés comme les composantes d’un continuum formant une même famille de corps interstellaires. Ces comètes générées à proximité de Jupiter sont moins abondantes que celles qui ont été formées dans le nuage de Oort, même si elles étaient probablement beaucoup plus nombreuses au cours de la genèse du système solaire, avant d’être éjectées du système solaire en raison du champ de gravité énorme imposé par Jupiter. Ces comètes joviennes ont aussi une espérance de vie courte, de l’ordre de 1,5×105 ans, ce qui réduit fortement la probabilité d’impacts avec la jeune Terre. Plus critique encore est le résultat du calcul du nombre minimal de comètes nécessaire pour aboutir au montant estimé de l’eau stockée sur la Terre. Comme on le verra au chapitre 4, il y a une grande quantité d’eau disséminée dans le manteau de la Terre, les estimations allant d’une masse identique à celle des océans à une masse cinq fois supérieure. En supposant qu’il n’y a pas eu de pertes d’eau lors des violents impacts cométaires, un scénario lui-même peu probable, un simple calcul du bilan de masse suggère qu’environ cinquante millions de ces comètes auraient été nécessaires pour expliquer la masse totale d’eau terrestre. Nous allons voir d’autres théories concurrentes expliquant l’origine de l’eau sur Terre, impliquant d’autres sources et mécanismes de fourniture de l’eau à notre planète.
3. Les chondrites carbonées et les astéroïdes de glace
Parmi les différentes familles de météorites, les chondrites carbonées et en particulier le groupe CI, contiennent une grande quantité d’eau allant de 3 à 22 % en poids, en plus de molécules organiques comme des acides aminés (figure 5). Ces météorites sont principalement constituées de silicates anhydres, comme l’olivine ou hydratés, comme la serpentine et les argiles. Ils contiennent également des oxydes riches en fer tels que la magnétite et des sulfures en faible quantité. Ces chondrites carbonées n’ont jamais été exposées à des températures supérieures à 50 °C et on considère généralement que leur composition chimique globale reflète fidèlement celle de la nébuleuse protosolaire.
Figure 5. Echantillon de chondrite carbonée
(source : collection de l’Ecole normale supérieure de Lyon, France)
Ces météorites sont des restes des corps parentaux ou planétésimaux qui ont contribué à former la Terre (figure 6). L’accroissement de la taille de la Terre a été assuré par accrétion de ces planétésimaux, phénomène au cours duquel l’énergie gravitationnelle a été convertie en énergie thermique, d’abord par l’impact, puis par le processus de compression de la matière. Les températures de la Terre sont alors devenues suffisamment élevées pour faire fondre totalement les roches. Une source auxiliaire de chaleur interne, aujourd’hui encore en activité, a été la désintégration des isotopes radioactifs présents dans les minéraux des roches, en particulier le potassium. Alors que les éléments les plus lourds tels que Ni et Fe se sont différenciés et ont plongé pour former le noyau métallique de la Terre, les éléments les plus légers ont eux migré vers la surface pour former les enveloppes fluides externes.
Figure 6. Vue d’artiste du phénomène d’accrétion des planètes telluriques
de notre système solaire
Les bilans de masse, chimique et isotopique, de l’oxygène impliquent que la plupart des corps parentaux (≈ 98 %), qui ont formé les enveloppes solides de la Terre, ont été des matériaux anhydres, comme par exemple l’enstatite (MgSiO3) des chondrites. Cependant, la plupart des fluides, y compris toute l’eau de la Terre, auraient pu provenir du dégazage à haute température de seulement 2 % des chondrites carbonées ou des astéroïdes de glace accrétés pour former la Terre (figure 7), ces deux types de corps parentaux ayant circulé à l’intérieur de la ceinture d’astéroïde entre Mars et Jupiter. Selon les modèles de différenciation de la Terre, en particulier ceux qui envisagent la ségrégation du noyau, la distribution de l’eau à la surface de la Terre et, par conséquent, la formation des océans de la planète, a eu lieu entre 50 et 200 millions d’années après la fin de l’accrétion de la Terre.
Figure 7. Vue d’artiste de l’astéroïde de glace Cybèle
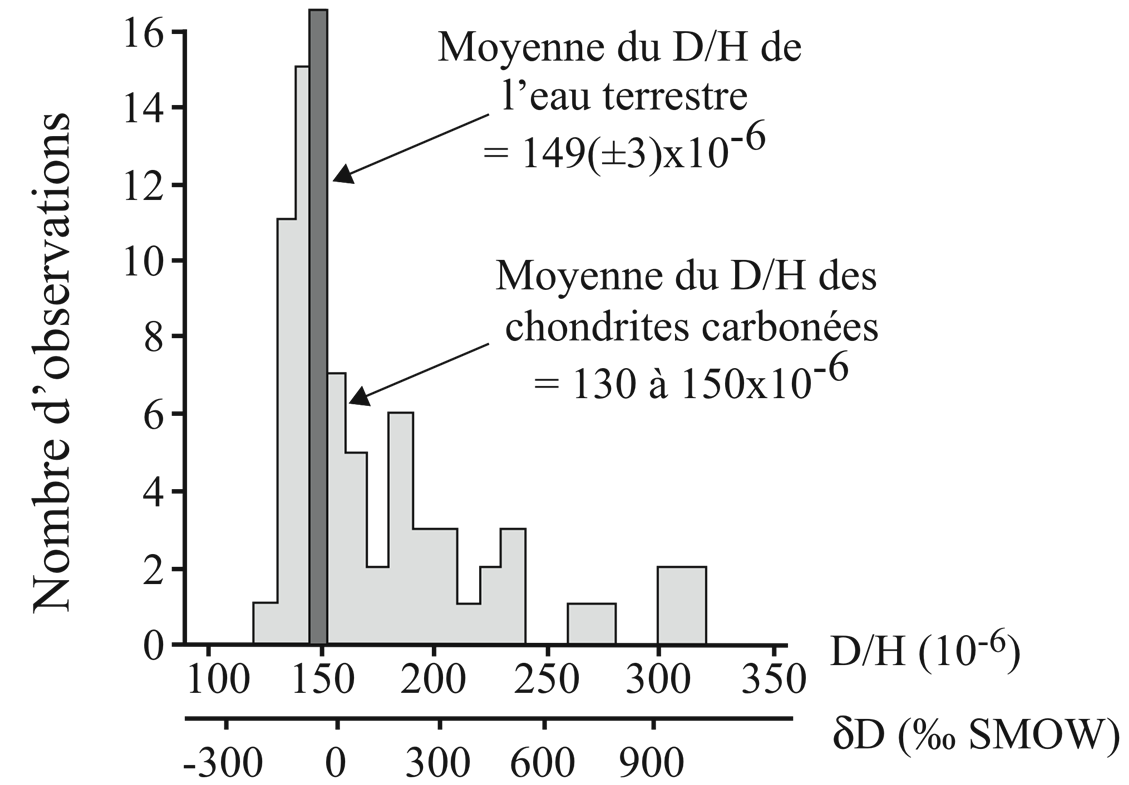
On peut donc accepter l’hypothèse d’une contribution mineure de l’eau cométaire au volume total de l’eau de la Terre, au moins 90 % en poids de cette eau provenant de ces petits astéroïdes ayant une composition chondritique carbonée primitive. En outre, les chondrites carbonées ont des rapports iotopiques D/H dans la gamme 130 à 200×10-6 avec une valeur moyenne de 149±6×10-6 (figure 8), valeur qui est similaire à la moyenne estimée du rapport D/H global de la Terre (149 ± 3×10-6).
Figure 8. Rapports D/H de l’eau des chondrites carbonées comparés
à la valeur moyenne du D/H de la Terre (figure d’après Lécuyer et al. [LEC 98])
Une théorie alternative soutient le concept de formation de la Terre par accrétion de « grains solides humides » qui aurait pu contenir d’une à trois fois la quantité d’eau nécessaire à la formation des masses océaniques. L’idée que l’eau sur Terre pourrait provenir de l’adsorption de l’eau de la nébuleuse sur des grains dans le disque d’accrétion, eau qui aurait survécu au processus d’accrétion reste cependant hautement spéculative. De plus, comme l’efficacité de l’adsorption d’eau sur un solide augmente à mesure que la température diminue, on s’attendrait à ce que Mars ait piégé proportionnellement plus d’eau que la Terre, et la Lune aurait dû recevoir de grandes quantités d’eau alors qu’il est parfaitement connu qu’elle en est dépourvue, au moins jusqu’à environ 500 km de profondeur. Il existe des preuves de la présence d’eau sur Mars, révélées par l’analyse des rayons gamma et par les spectromètres à neutrons qui étaient embarqués à bord du vaisseau spatial Mars Odyssey. Des abondances élevées en hydrogène ont été interprétées par l’existence de couches de glace d’au moins un mètre d’épaisseur enfouies sous une couche de poussière basaltique à des latitudes supérieures à 60° dans les deux hémisphères. Cette théorie se dispense de la nécessité de faire appel à des minéraux riches en eau comme ceux présents dans les chondrites carbonées. Les conséquences sur l’évolution précoce de la Terre sont également essentielles dans le cadre de cette théorie de l’accrétion de solides humides. L’eau abaisse en effet le point de fusion des silicates et ceci devrait alors avoir favorisé l’existence d’un océan de magma en profondeur. En outre, la présence très précoce de grandes quantités d’eau devrait avoir des conséquences critiques sur l’évolution de l’état redox de la planète, avec des taux d’oxydation plus élevés des composants du manteau et du noyau par rapport à une planète principalement née de l’accrétion de solides anhydres.
Dans le cadre de cette hypothèse alternative, on peut supposer que le rapport isotopique D/H des océans terrestres présente une valeur qui résulte d’un équilibre fortuit entre celle de l’eau provenant de la nébuleuse solaire et celle de l’eau enrichie en deutérium, provenant des comètes. Une équation de bilan de masse peut être établie en égalant l’état initial (terme de gauche) avec l’état final (terme de droite) de la distribution de l’eau et des rapports isotopiques D/H entre les réservoirs mantelliques et océaniques :
En utilisant les données rappelées ci-dessous :
– masse de la Terre : Rfme = 5×1024 kg ;
– masse des océans actuels : Efoe = 1,38×1021 kg ;
– rapport isotopique D/H du manteau actuel : (D⁄H)fme = 1,432×10-4 ;
– rapport isotopique D/H du manteau primordial : (D⁄H)imp = 0,25×10-4 ≈ celui de la nébuleuse protosolaire ;
– rapport isotopique de l’océan actuel : (D⁄H)foe = 1,557×10-4 ;
– rapport isotopique de l’océan primordial : (D⁄H)iop = 3×10-4 ≈ celui des comètes de la famille de Oort :
[H20]fme = 100 ppm
Et sachant que :
Le bilan de masse est alors réalisé pour un manteau primordial contenant 180 ppm d’eau provenant de la nébuleuse solaire en supposant que le manteau évolué actuel a 100 ppm d’eau. Ces calculs demeurent hautement spéculatifs et il faut garder à l’esprit que la méthode du bilan similaire doit satisfaire à d’autres éléments volatils présents dans l’atmosphère, tels que l’azote.
4. L’évolution modérée du rapport isotopique D/H de l’océan mondial
Deux flux unidirectionnels affectent le bilan de l’eau sur la Terre : ce sont d’une part, un apport d’eau dû, on l’a vu, à des impacts de corps extra-terrestres et, d’autre part, une perte en eau due à la fuite de l’hydrogène atomique dans l’espace après photodissociation de l’eau dans la haute atmosphère. Considérons les conséquences de ces deux mécanismes sur le rapport isotopique D/H de l’océan depuis 4,5 milliards d’années.
La masse totale M(t) des corps météoritiques accumulés sur la Lune au cours des temps géologiques peut aisément être calculée grâce au traitement statistique de la densité observée des cratères d’impact lunaires en fonction du temps. Ce calcul, bien sûr, est impossible pour la Terre, mais la mise à l’échelle de M(t) par la section efficace gravitationnelle de la Terre, qui est 23 fois plus grande que celle de la Lune, permet d’obtenir une solution analytique :
Le temps t y est exprimé en milliards d’années, la surface de la Terre S en km2, et la masse totale de matériel extraterrestre M(t) en kg. On obtient ainsi la relation :
M(H2O) = M(t)[(1–x)(0,95)(0,90)(0,50)(0,10) + (x)(0,85)(0,50)(0,50)]
où (x) est la part relative de météorites dans le flux extraterrestre et (1–x), la part due aux comètes.
Dans le premier terme, 5 % de la masse des océans ont été perdus lors des impacts, 90 % du corps impactant s’est accrété à la Terre et, parmi les météorites, 50 % sont riches en eau, avec des concentrations atteignant 10 % en poids.
Le second terme traduit la contribution cométaire, 15 % de la masse des océans étant perdus dans l’espace lors des impacts, 50 % des comètes s’accrétant à la masse terrestre, avec une concentration en eau de 50 % en poids.
En prenant en compte ces paramètres, l’application numérique montre que la masse totale d’eau M(H2O) ajoutée aux océans terrestres pendant 4,5 milliards d’années devrait se situer entre 4 % et 22 % selon la contribution relative des comètes et des chondrites carbonées riches en eau. Selon ce calcul, respectivement 0,01 %, 0,1 % et 1 % d’eau extraterrestre ont été ajoutés à la Terre depuis 1, 3,8 et 4,2 milliards d’années, respectivement. En utilisant le rapport isotopique D/H de la comète P/Halley, les valeurs de δD des océans étaient respectivement de –0,2, –3,0 et –11 ‰ à 1, 3,8 et 4,2 milliards d’années (voir au chapitre 1 la relation entre le rapport D/H et la valeur δD normalisée au SMOW, Standard Mean Ocean Water).
La variation maximale possible du rapport isotopique des océans terrestres due aux toutes dernières additions d’eau extraterrestre peut également être calculée. En mettant à l’échelle l’équation ci-dessus afin d’obtenir une entrée d’eau extraterrestre totale égale à la masse actuelle de l’eau sur Terre, le flux maximum possible de l’eau extra-terrestre peut être calculé. Si le flux d’eau extraterrestre intégré était douze fois plus important que celui estimé par l’équation ci-dessus, alors on aurait M(H2O)/M(océans) = 1 pour t = 4,5 milliards d’années. Une telle sous-estimation d’un facteur 12 correspond aux limites supérieures des barres d’erreur définies pour le flux extraterrestre ; en d’autres termes M(H2O)/M(océans) = 1 n’est pas déraisonnable compte tenu de l’incertitude associée aux données obtenues à partir de la connaissance de la cratérisation de la surface lunaire. Compte tenu des changements isotopiques pour les roches terrestres connues les plus anciennes (d’âges ≤ 4,0 milliards d’années) et en supposant que toute l’eau ajoutée à la Terre depuis l’époque avait un rapport D/H similaire à celui des comètes, le δD calculé des océans terrestres présentait les valeurs respectives suivantes : –3,7 ‰, –6,1 ‰ et –66,6 ‰ (SMOW) il y a respectivement 3,0, 3,5 et 4,0 milliards d’années. On peut donc conclure que la variation de composition isotopique des océans causée par une possible addition d’eau extraterrestre sur Terre est négligeable depuis au moins 3,5 milliards d’années.
5. Composition chimique des océans de la Terre primordiale
5.1. L’énorme effet de serre qu’a connu la Terre primitive
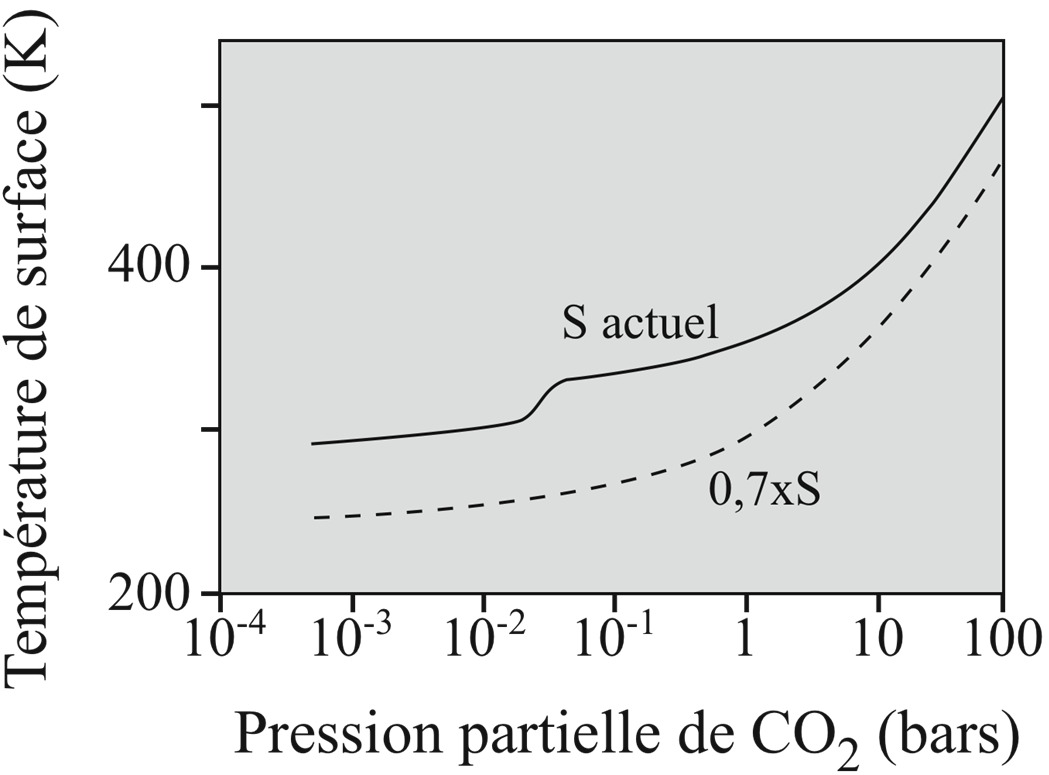
La preuve de la présence précoce des océans sur Terre est fournie par les plus anciennes roches sédimentaires. Des restes de sédiments marins pélagiques ont été découverts à Isua, au Groenland, datés de 3,7×109 années. Le site d’Akilia, également au Groenland, a fourni des sédiments très anciens datés à 3,86 ± 0,11×109 ans, caractérisés par des minéraux et une composition chimique hors du commun. Ces sédiments, composés de magnétite (Fe3O4) et de quartz (SiO2) sont appelés Banded Iron Formation (BIF) (formation de fer rubanée) et témoignent du fait que les océans primordiaux présentaient une composition chimique radicalement différente de celle qui prévaut depuis le début des temps phanérozoïques (il y a environ 550 millions années). Les océans primordiaux ont été en contact avec une atmosphère ayant une pression partielle de CO2 d’environ 100 bars, équivalent au stock estimé (≈ 5,4×1019 kg de C) du carbone aujourd’hui stocké soit dans les roches carbonatées, soit sous forme de matière organique (charbon, pétrole, gaz). A ces réservoirs su-perficiels, il faut ajouter une quantité de carbone prise au piège dans les plaques lithosphériques océaniques lors du processus de subduction, qui correspond à environ 25 ppm de carbone dans le manteau terrestre actuel. Ces teneurs considérablement élevées de dioxyde de carbone atmosphérique dans l’atmosphère de la Terre primitive étaient responsables d’un effet de serre énorme, avec des températures de surface pouvant atteindre 400°C (figure 9).
Figure 9. Variations de la température de surface de la Terre primitive (en °C) en fonction de la pression partielle de CO2 dans l’atmosphère (en bars). Les calculs de températures tiennent compte du fait que la luminosité solaire était réduite de 30 % par rapport à celle que nous connaissons depuis les temps phanérozoïques et que l’atomphère ne contenait pas d’oxygène (extrait de Kasting and Ackerman [KAS 86]).
5.2. Le pH et l’état redox de l’océan terrestre primordial
Ces importantes pressions partielles de CO2, associées à l’absence d’oxygène moléculaire dans l’atmosphère, permettent de conclure que les eaux océaniques de ces périodes étaient d’une part anoxiques (sans O2 dissous) et d’autre part nettement acides (pH < 5). Ces déductions sont en parfait accord avec les conditions nécessaires au dépôt des formations de fer rubanées au Protérozoïque lorsque les océans sont devenus basiques et un peu oxygénés, entre 2,5 et 2,0 milliards d’années.
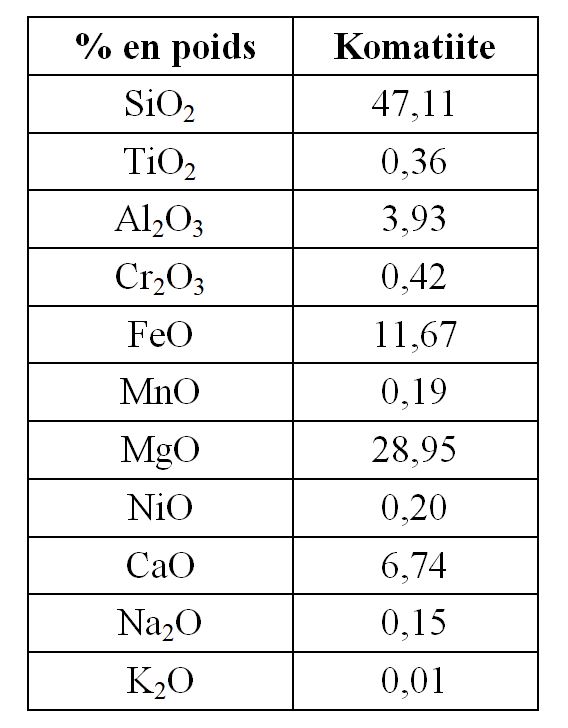
En effet, ces sédiments marins riches en fer (avec des minéraux comme la magnétite Fe3O4) et riches en silice (présence de chert) témoignent, avant leur précipitation, de teneurs élevées en Fe2+ soluble dans les eaux de mer archéennes, teneurs uniquement compatibles avec des eaux privées d’oxygène dissous et caractérisées par un pH bas, dans la gamme 0 à 6. A cette époque, en l’absence de continents, la chimie de l’eau de mer a été très probablement contrôlée par des réactions entre l’eau et les roches magmatiques volcaniques du fond des océans, à haute température (300-600°C). En raison d’un gradient géothermique élevé prévalant au cours de l’Archéen, ce qui reflète un flux de chaleur interne plus élevé, ces roches volcaniques sont nées de la fusion des péridotites mantelliques à des températures très élevées, de l’ordre de 1 700°C au lieu des 1 200°C que l’on observe aujourd’hui dans les volcans. A des températures aussi élevées, les silicates fondus contiennent davantage de Mg (voir le tableau 1 pour la composition chimique), cristallisé sous forme de silicates appelés forstérites (Mg2SiO4), composants principaux des roches appelées komatiites (figure 10), associés à des pyroxènes calciques ((Ca, Na)(Mg, Fe, Al, Ti)(Si, Al)2O6) et des chromites comme composant mineur (Fe2+Cr2O4). Ces komatiites sont des roches ultramafiques ainsi nommées d’après leur découverte par M. et R. Viljoein le long de la vallée de la rivière Komati, en Afrique du Sud.
Tableau 1. Composition chimique en éléments majeurs d’une lave komatitique
de la formation Barberton Greenstone Belt, Afrique du Sud, datée de 3,45 milliards d’années
Figure 10. Lave komatitique d’Ontario, Canada, qui révèle une structure spinifex typique (texture dendritique, semblable à celle des aiguilles de pins), reflétant un refroidissement rapide au contact de l’eau d’un magma chaud (1 500–1 700°C) et riche en Mg (25-30 % en poids)
5.3. Les roches ultramafiques archéennes, un piège pour le CO2 atmosphérique de la Terre primitive
Après cette période très chaude de la Terre primitive, l’abaissement de la température a été intimement lié à la décroissance de l’effet de serre induit par la pression partielle de CO2 atmosphérique. Une voie possible qui a conduit à diminuer la pression partielle de ce gaz a été de le piéger dans les roches sédimentaires selon des réactions chimiques à haute température qui sont intervenues entre les laves ultramafiques komatitiques et l’eau de mer archéenne. En effet, les assemblages minéralogiques métamorphiques ou secondaires résultant de ces interactions fluide-roche dépendent de la pression partielle en CO2. En dessous de 0,5 atmosphère, les minéraux formés sont la trémolite, le talc et la magnésite (MgCO3). Dans les conditions sous-marines, les minéraux formés sont la serpentine, la chlorite et la brucite (Mg(OH)2), qui se substituent à la forstérite (Mg2SiO4) et à l’enstatite (MgSiO3).
La chimie des eaux des sources naturelles qui se sont infiltrées dans des roches ultramafiques est bien documentée. La grande solubilité de la forstérite et de l’enstatite est responsable d’une augmentation du pH ainsi que de fortes teneurs en Mg2+ des solutions aqueuses, selon les réactions :
Mg2SiO4 + 4H+ ➔ 2Mg2+ + H4SiO4
MgSiO3 + 2H+ + H2O ➔ Mg2+ + H4SiO4
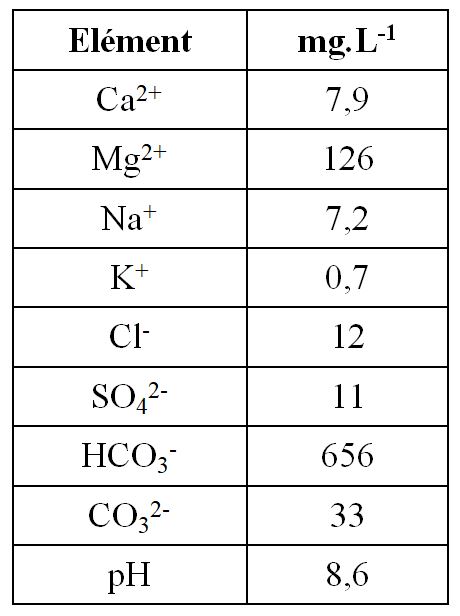
Ces eaux sont en conséquence alcalines, avec des pH compris entre 8 et 9 et la spéciation chimique du carbone s’exprime sous forme d’ions bicarbonates et carbonates, ainsi que l’on peut le constater sur les valeurs de compositions chimiques d’eaux de source issues de roches ultramafiques (tableau 2).
Tableau 2. Compositions chimiques moyennes en mg.L-1 des eaux riches en Mg2+ et en
HCO3– associées à des massifs de roches ultramafiques aux Etats-Unis.
Données issues de Barnes et O’Neil [BAR 69]
Dès que la sursaturation de la solution est atteinte, les ions bicarbonates et magnésium précipitent sous forme de magnésite (figure 11), selon la réaction :
HCO3– + Mg2+ ➔ MgCO3 + H+
La précipitation de carbonate de calcium peut également se coproduire lors de la dissolution de pyroxènes calciques, produisant de la trémolite, et libérant des ions Ca2+ :
4(Ca, Mg)Si2O6 + Mg2+ + 2H+ ➔ Ca2Mg5(Si8O22)(OH)2 + 2Ca2+
Figure 11. Veines de magnésite dans des roches ultramafiques serpentinésées,
nord de Magurë, Kosovo (source de la photo : site web de l’Independent Commission
for Mines and Minerals (ICMM), Kosovo)
5.4. La salinité de l’océan terrestre primordial
A l’Archéen, les continents étaient encore très peu développés, leur taille ne devant probablement pas dépasser 10 à 20 % de leur taille actuelle et ceci avait pour conséquence que la chimie de l’eau des océans devait être tamponnée par le manteau terrestre, via les échanges chimiques se produisant lors des interactions hydrothermales avec la croûte océanique. Par conséquent, on peut s’attendre à ce que l’eau de mer archéenne était plus riche en éléments alcalins et alcalino-terreux tels que Na+, K+, Mg2+, Ca2+ et Sr2+, qui se sont progressivement accumulés dans la croûte continentale en pleine croissance. Dans les océans modernes, depuis environ la fin du Jurassique ≈ 150 millions d’années, le Ca2+ est utilisé par de nombreuses espèces d’organismes sécrétant une coquille carbonatée, ce qui explique les faibles quantités relatives de calcium dissous dans les océans (voir chapitre 3). De même, la silice dissoute était probablement abondante dans les océans archéens tandis que le chlore présentait des concentrations proches de celle des océans modernes en raison de sa forte solubilité.
Dans les eaux anoxiques de cet océan primordial, les ions sulfates, provenant de gaz volcaniques tels le SO2 étaient facilement réduits par le Fe2+ dissous et précipitaient sous forme de sulfure de fer comme la pyrite (FeS2). La présence d’ions sulfate ne nécessite pas la présence d’oxygène libre car le SO2 réagit avec l’eau pour former H2SO4, même à des températures de 200°C. La spéciation de l’azote privilégiait l’ammonium NH4+ au lieu des nitrates NO3–, comme dans les océans actuels. En effet, la présence de nitrates dans l’eau de mer est maintenant liée à l’élévation des teneurs en O2 dans l’atmosphère il y a environ deux milliards d’années, rendant possible l’oxydation de l’ammonium par des bactéries chimiotrophes nitrifiantes. Dans les océans archéens, de nombreux micro-organismes de type archées se sont adaptés à ces milieux aquatiques chauds, acides et anoxiques. Ces procaryotes forment plusieurs groupes métaboliques, dont trois au moins présentent un grand intérêt dans le cadre du présent chapitre. Un premier comprend les méthanogènes, connus actuellement pour être associés aux sources hydrothermales des dorsales océaniques, et qui produisent du méthane à partir de dioxyde de carbone selon la réaction chimique suivante :
CO2 + 4H2 ➔ CH4 + 2H2O
Le second groupe est celui des halophiles qui investissent des environnements hypersalins, depuis 90 g.L-1 jusqu’à la sursaturation en NaCl, environnements tels que ceux que l’on observe actuellement dans la Mer Morte. Le troisième groupe réunit les micro-organismes qui métabolisent le soufre, comme par exemple Sulfolobus, une Archaea thermophile qui est observée dans les eaux associées aux volcans, où elle se développe idéalement à un pH de 3 et à des températures de 75-80°C. Ce micro-organisme est capable d’oxyder le soufre natif en acide sulfurique :
2S0 + 3O2 + 2H2O ➔ 2H2SO4
Ces organismes métaboliseurs du soufre ont très probablement joué un rôle important dans le cycle du soufre, lorsque la teneur en oxygène moléculaire a commencé à augmenter à la surface de la Terre.
6. Bibliographie
[ALB 09] Albarède F., « Volatile accretion history of the terrestrial planets and dynamic implications », Nature, vol. 46, p. 1227-1233, 2009.
[ALB 13] Albarède F., Ballhaus C., Blichert-Toft J., et al., « Asteroidal impacts and the origin of terrestrial and lunar volatiles », Icarus, vol. 222, p. 44-52, 2013.
[BAR 69] Barnes I., O’Neil J.R., « The relationship between fluids in some fresh alpine–type ultramafic rocks and possible modern serpentinization, western United States », Geological Society of America Bulletin, vol. 80, p. 1947-1960, 1969.
[DRA 05] Drake M.J., « Origin of water in the terrestrial planets », Meteoritics and Planetary Science, vol. 40, p. 519-527, 2005.
[HAL 13] Halliday A.N., « The origins of volatiles in the terrestrial planets », Geochimica et Cosmochimica Acta, vol. 105, p. 146-171, 2013.
[HAR 11] Hartogh P., Lis D.C., Bockelée-Morvan D., et al., « D/H ratios in the Solar System », Nature, vol. 478, p. 218-220, 2011.
[HOR 07] Horner J., Mousis O., Hersant F., « Constraints on the formation regions of comets from their D:H ratios », Earth, Moon, and Planets, vol. 100, p. 43-56, 2007.
[HUN 74] Hunten D.M., McElroy M.B., « Production and escape of terrestrial hydrogen », Journal of the Atmospheric Sciences, vol. 31, p. 305-317, 1974.
[JAC 13] Jacquet E., Robert F., « Water transport in protoplanetary disks and the hydrogen isotopic composition of chondrites », Icarus, vol. 223, p. 722-732, 2013.
[JAV 98] Javoy M., « The birth of the Earth’s atmosphere: the behaviour and fate of its major elements », Chemical Geology, vol. 147, p. 11-25, 1998.
[KAS 86] Kasting J.F., Ackerman T.P., « Climatic consequences of very high carbon dioxide levels in the Earth’s early atmosphere », Science, vol. 234, p. 1383-1385, 1986.
[LEC 98] Lécuyer C., Gillet P., Robert F., « The hydrogen isotope composition of seawater and the global water cycle », Chemical Geology, vol. 145, p. 249-261, 1998.
[LEC 00] Lécuyer C., Simon L., Guyot F., « Comparison of carbon, nitrogen and water budgets on Venus and the Earth », Earth and Planetary Sciences, vol. 181, p. 33-40, 2000.
[MAR 12] Marty B., « The origins and concentrations of water, carbon, nitrogen and noble gases on Earth », Earth and Planetary Science Letters, vol. 313-314, p. 56-66, 2012.
[PIN 05] Pinti D.L., « The origin and evolution of the oceans », dans M. Gargaud, et al. (dir.), Lectures in Astrobiology, vol. 1, p. 83-112, Springer-Verlag, Berlin Heidelberg, 2005.
[ROB 82] Robert F., Epstein S., « The concentration and isotopic composition of hydrogen, carbon and nitrogen in carbonaceous meteorites », Geochimica et Cosmochimica Acta, vol. 46, p. 81-95, 1982.
[ROB 06] Robert F., « Meteorites and the early Solar System II », dans D.S. Lauretta, H.Y. McSween Jr. (dir.), University of Arizona Press, Tucson, vol. 943, p. 341-351, 2006.
Pour en savoir plus : L’eau sur la Terre